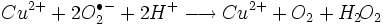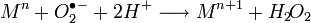Wikipedia:
Superoxide dismutase is een
essentieel enzym dat
zuurstofradicalen in organismen 'opruimt'. De reactie die
het enzym versnelt is voor zover bekend de allersnelste in de
biochemie. Superoxide dismutase is een klasse van enzymen,
welke een aantal verschillende metaalkernen kunnen hebben als
actief centrum. Dit kan ijzer, koper/zink, mangaan of nikkel
zijn. Het is afhankelijk van het gebruikte metaal welke
ligandomgeving er is. De koper/zink variant is het effectiefst
voor zover bekend. De koper/zink superoxide dismutase versnelt
de volgende reactie:
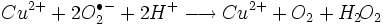
De overall-reactie bestaat in feite uit
de volgende twee reacties:

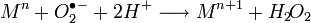
Opvallend hierbij is dat het enzym zowel
Cu (I) als Cu(II) laat reageren met superoxide, het
zuurstofradicaal. Hierdoor kan het enzym altijd actief zijn,
zowel met een eenwaardig als met een tweewaardig koperatoom
gebonden in het enzym. Hierdoor kan de reactie zo supersnel
plaatsvinden. H2O2 wordt vervolgens
"opgeruimd" door
katalase, een enzym dat grofweg een factor 1000 langzamer
werkt als superoxide dismutase.
Het is overigens ook niet voor niets dat
superoxide dismutase zo snel reageert. Superoxide behoort
namelijk tot de reactiefste moleculen, en zou praktisch met
alles reageren wat het aan moleculen tegenkomt, dus ook met
bijvoorbeeld DNA. Het snel opruimen van de radicalen is dan ook
noodzakelijk. De radicalen komen zo nu en dan vrij als "ongeluk"
bij diverse reacties.
 |
 |

contact print
zoeken |
|
|
|
|
|
|
|
|
|
Metaalarbeider op
de gevoelige toer
Bron:
Nieuwsbrief Universiteit Leiden 5 juli 2005
|
Koperman
Biochemicus Armand Tepper
is, zoals hij zelf zegt, een
‘koperman’. Hij hoort bij de
onderzoeksgroep van prof. Gerard
Canters, waarin wordt gewerkt
aan metaaleiwitten. Dat zijn
eiwitten waaraan metaal-ionen
gebonden zijn. Het metaal maakt
dat het eiwit in een levende cel
een hele reeks van functies kan
uitvoeren, die voor eiwitten
zonder metaal meestal te hoog
gegrepen zijn. Haemoglobine in
het bloed is een bekend
voorbeeld van een
metaaleiwit, maar ook het
fotosynthetische systeem zit vol
met metalen. Ook bij het proces
dat energie uit suikers haalt
zijn veel metaaleiwitten
betrokken. |

Armand Tepper |
|
|
|
|
Helderblauw
Metaaleiwitten zijn niet alleen van
levens-belang in een organisme, maar
maken ook het leven van een
wetenschapper gemak-kelijker. Met
gebruik van metaaleiwitten kun je
namelijk een hele reeks spectroscopische
technieken toepassen die met gewone
eiwitten niet mogelijk zijn, zoals
speciale variaties op NMR. Een voordeel
is alleen al dat metaaleiwitten een
mooie kleur hebben, waardoor ze goed te
onderscheiden zijn. ‘Wij zien de mooiste
kleuren’, zegt Tepper. ‘Vooral koper en
ijzer zijn heel mooi. Hae-moglobine is
diep rood. En bepaalde koper-eiwitten
hebben een prachtige helderblauwe
kleur.‘ |

Metaaleiwitten hebben vaak een
kleur.
Links nitriet reductase en rechts
pseudoazurine, beide kopereiwitten |
|
|
Bionanotechnologie
Met die spectroscopische
technieken kunnen onderzoekers meer te
weten komen over de functie van het
metaal in het eiwit. Heel precies op
atomair niveau kunnen ze tegenwoordig de
mechanismen van eiwitten ontrafelen.
Tepper: ‘Eiwitten zijn grote en zeer
complexe moleculen. Maar we zijn nu
zover dat we een beetje begrijpen hoe
het werkt, en dat we die kennis ook
kunnen toepassen. Dan zit je op het
terrein van de bionanotechnologie.’
Elektronenverkeer
Een van de eigenschappen van
metaaleiwitten is dat ze
elektronenverkeer mogelijk maken als ze
reageren met andere stoffen: ze nemen
elektronen op of staan ze af. Dat
gebeurt tijdens de zogenoemde
redox-processen. ‘Redox’ is een
samentrekking van reductie en oxidatie.
Het molecuul dat een elektron afstaat
heet geoxideerd, en het molecuul dat er
een elektron bij krijgt heet
gereduceerd.
Biosensor
Tepper zelf gaat kopereiwitten
inzetten als hulpmiddel om een radicaal
nieuwe procedure te testen voor het
maken van een biosensor. Daarbij maakt
hij gebruik van die redox-processen. Een
biosensor is een sensor waarin
biologische elementen zijn geïntegreerd.
Biosensoren zijn handig, want
biologische moleculen zijn heel
specifiek. Tepper: ‘Neem de bekendste,
de glucosesensor, waarmee glucose
gemeten kan worden in het bloed. Die is
gebaseerd op een gespecialiseerd eiwit
dat in het lichaam glucose
metaboliseert. Zo’n eiwit heeft dus als
enige
target dat glucosemolecuul. Een
biosensor op basis van dat eiwit
is daarom een heel gerichte detector,
die allerlei ballast buiten beschouwing
laat.’ |
Elektrisch stroompje
Er is op het ogenblik veel
belangstelling voor metaaleiwitten als
component van een biosensor, juist
vanwege die elektronen-overdracht bij
chemische reacties. Die maakt namelijk
heel eenvoudige detectiemethoden
mogelijk, zegt Tepper.
‘Elektronenoverdracht betekent: een
elektrisch stroompje. En een elektrisch
stroompje kun je vrij gemakkelijk
meten.’ Om een biosensor te maken
immobiliseert Tepper een kopereiwit op
een vaste drager. Naar dat eiwit stuurt
hij elektronen toe met behulp van een
elektrode. Met die elektroneninjectie
lokt hij een chemische reactie uit van
het eiwit met het molecuul dat hij wil
detecteren. In zijn geval is dat
nitriet. |

Het principe achter een biosensor
gebaseerd op redoxeiwitten |
| |
|
Nitriet
Nitriet, bekend van voedselindustrie
en afvalwater, is een klein maar
belangrijk molecuul in levende cellen.
Het bestaat uit één stikstofatoom en
twee zuur-stofatomen. Nitriet wordt
spontaan gevormd bij de afbraak van NO,
stikstof-monoxide. De
nitrietconcentratie is dus een maat voor
de hoeveelheid afgebroken NO. En NO is
het molecuul waar het Tepper eigenlijk
om te doen is.
Mystery Molecule
Werd stikstofmonoxide (NO) vroeger
uitsluitend gezien als een giftig
uitlaatgas, sinds de tweede helft van de
jaren ‘80 is bekend dat dit gas een
signaalfunctie heeft bij heel veel
cruciale fysiologische processen. Het
reguleert bijvoorbeeld de bloeddruk, en
speelt daarom een belangrijke rol in het
onderzoek. Al deze
ontdekkingen hebben geleid tot een ware NO-hype in het onderzoek, culminerend in
een Nobelprijs in 1998. Het probleem met
deze ‘mystery molecule’ is dat
hij binnen tien seconden wordt
afgebroken in het bloed. Maar daarbij
komt dus het nitriet vrij dat Tepper
graag wil meten. Het gespecialiseerde
kopereiwit dat hij in zijn biosensor
gebruikt is nitriet reductase, dat in de
natuur betrokken is bij de omzetting van
nitriet.Isolator
Maar als dit het enige was zou
Tepper zijn Veni-subsidie helemaal niet
nodig hebben. Er is echter een probleem:
het metaalcentrum zit heel diep in het
eiwit opgeborgen. In de natuur heeft dat
een functie: de eiwitlaag wordt benut
ten behoeve van de specificiteit,
bijvoorbeeld voor de herkenning van een
ander eiwit. Of om alleen dát molecuul
aan het metaal te laten binden dat moet
worden omgezet. Elektronoverdracht is zo
alleen mogelijk door interactie met
specifieke partnermoleculen, terwijl
onbedoelde processen worden voorkomen.
Maar voor een wetenschapper is het
daardoor heel moeilijk om een stroom
elektronen te laten lopen van de
elektrode naar het metaal in het eiwit;
het eiwit werkt als een isolator. Dit
principiële probleem, zegt Tepper, heeft
een vertragende werking gehad op de
ontwikkeling van biosensoren die
gebaseerd zijn op redox-eiwitten. Wat
hij dus gaat doen is een radicaal nieuwe
methode testen om dat probleem aan te
pakken.
Patent
Hoe hij die eiwit-weerstand denkt te
gaan overwinnen kan hij op dit moment
nog niet zeggen, hoewel hij er alle
vertrouwen in heeft dat het gaat lukken.
Beter gezegd: juist omdat
hij daar alle vertrouwen in heeft.
Interdisciplinair
Na een onderzoeksperiode in Napels
is Tepper terug in de
metaaleiwittengroep van Gerard Canters,
bij wie hij in maart promoveerde op een
ander kopereiwit. In die groep voelt hij
zich thuis. Er zijn in Nederland niet
zoveel groepen die gespecialiseerd zijn
in metaaleiwitten. Het is daarbij een
heel goede groep, vindt hij. Juist op
het gebied van die kopereiwitten. Met
zijn onderzoek komt Tepper steeds meer
in interdisciplinair vaarwater terecht,
wat hij als pure winst beschouwt. Vooral
de bionanotechnologie ziet hij als zijn
tweede vaderland. ‘Al heel lang voel ik
de behoefte om meer toegepast onderzoek
te doen. Ik denk heel erg technisch, en
ik houd van het oplossen van
technologische problemen.’ |
|
|
3D
Ook in zijn vrije tijd is Armand
Tepper met scheikunde bezig, maar dan op
een artis-tieke manier. Hij heeft altijd
veel geschilderd, en raakte gaandeweg
geïnteresseerd in het maken van
driedimensionale beelden op de computer:
fotorealistische afbeeldingen van
moleculen. ‘Je kunt wetenschap zo
artistiek maken als je wilt’, vindt hij.
Het was gewoon een hobby, maar van het
een kwam het ander, en steeds vaker
weten belangstel-lenden hem te vinden.
Hij werkt nu samen met zijn vriending
die grafisch vormgever is.
Zie voor meer artistiek werk:
www.phantatomix.com/whatwedo.htm |

Artistieke impressie van het actieve
centrum van het enzym CuZn superoxide
dismutase |
|
|
|
| Bron: Bart Meijer van
Putten. |
.